Dalle microonde alla risonanza magnetica: nanoparticelle più chiare, stabili e sicure per la diagnostica medica del futuro
Negli ultimi anni la diagnostica per immagini ha trasformato la medicina, rendendo visibile ciò che fino a poco tempo fa restava invisibile. Tra le tecniche più avanzate c’è la risonanza magnetica (MRI), uno strumento fondamentale per esplorare l’interno del corpo umano senza ricorrere a radiazioni o interventi invasivi. Tuttavia, per ottenere immagini nitide e dettagliate, la MRI necessita di “agenti di contrasto”, sostanze che migliorano la distinzione tra diversi tessuti e rendono più leggibili le strutture interne. Gli agenti più efficaci sono spesso a base di nanoparticelle magnetiche, piccolissime particelle di ossido di ferro, mille volte più piccole di un granello di sabbia, capaci di interagire con i campi magnetici. Ma nonostante i progressi, molti materiali finora utilizzati presentano limiti importanti: tendono ad aggregarsi, a degradarsi nel tempo o a interagire in modo indesiderato con le cellule. Da queste difficoltà è partita la ricerca di un ampio gruppo dell’Università di Torino, formato da Federica Calsolaro, Francesca Garello, Eleonora Cavallari, Giuliana Magnacca, Mikhail V. Trukhan, Maria Carmen Valsania, Giancarlo Cravotto, Enzo Terreno e Katia Martina, che ha ideato un nuovo modo per produrre nanoparticelle magnetiche più stabili, più sicure e più efficaci, pubblicato su Nanoscale Advances della Royal Society of Chemistry.
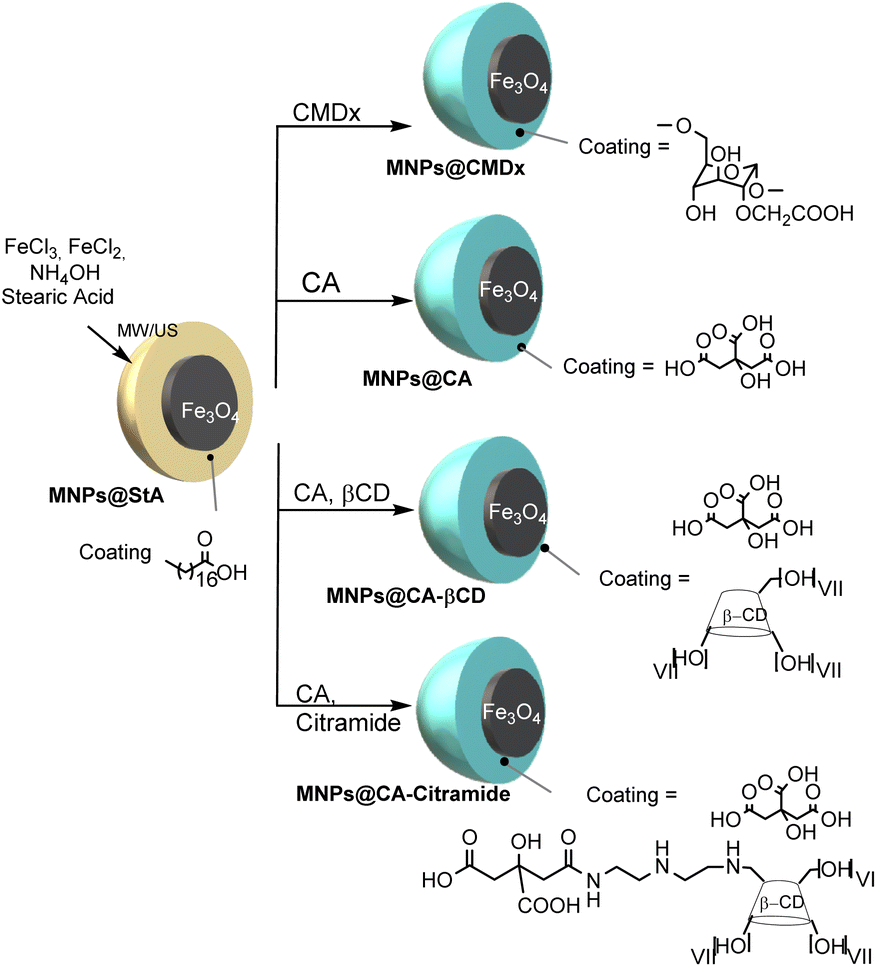
L’idea alla base della ricerca è tanto semplice quanto ingegnosa: usare due tecniche fisiche – microonde e ultrasuoni – non più solo come strumenti di laboratorio, ma come strumenti di sintesi dei materiali. Le microonde, le stesse che scaldano in modo rapido e uniforme il cibo, riscaldano i reagenti chimici in modo omogeneo, evitando differenze di temperatura che possono danneggiare la qualità del materiale. Gli ultrasuoni, invece, generano vibrazioni ad alta frequenza che creano piccole bolle di gas nel liquido, le quali, implodendo, producono microscopici vortici capaci di mescolare le sostanze e frammentare eventuali aggregati. Combinando queste due forze fisiche, i ricercatori hanno ottenuto un effetto sinergico: il calore delle microonde accelera le reazioni chimiche, mentre gli ultrasuoni mantengono il sistema in costante movimento, impedendo la formazione di grumi. In questo modo si ottengono nanoparticelle molto più uniformi, con dimensioni controllate – inferiori a 90 nanometri – e una carica superficiale stabile e negativa che impedisce loro di aggregarsi, rendendole idrofile e perfettamente disperdibili in soluzioni biologiche.
Il rivestimento delle nanoparticelle, cioè la parte esterna che ne determina il comportamento nei tessuti, è stato progettato con grande attenzione. Il gruppo torinese ha scelto due sostanze naturali: la β-ciclodestrina e l’acido citrico. La β-ciclodestrina è un composto zuccherino derivato dall’amido, con una struttura ad anello che funziona come una piccola gabbia molecolare capace di “ospitare” altre molecole al suo interno. Questa caratteristica le permette di catturare farmaci o molecole specifiche e rilasciarle in modo controllato. L’acido citrico, lo stesso che si trova negli agrumi, agisce invece come stabilizzante: si lega alla superficie del ferro impedendo alle particelle di fondersi tra loro e creando una barriera che le mantiene separate e stabili. Insieme, le due molecole formano una sorta di “pelle intelligente” attorno al nucleo magnetico, che rende le nanoparticelle compatibili con l’ambiente biologico e capaci di interagire con le cellule senza danneggiarle. Questa combinazione di chimica verde e tecnologia fisica ha dato vita a sistemi flessibili e multifunzionali, in grado non solo di migliorare la qualità delle immagini MRI, ma anche di trasportare molecole terapeutiche.
Per verificare il successo del nuovo metodo, i ricercatori hanno sottoposto le nanoparticelle a numerosi test di caratterizzazione. Le analisi di microscopia elettronica hanno mostrato che la dimensione e la forma delle particelle erano uniformi e regolari, mentre gli studi di magnetizzazione hanno rivelato un comportamento “superparamagnetico”. Questo termine, apparentemente complesso, significa che le particelle reagiscono ai campi magnetici solo quando sono presenti, ma non restano magnetizzate una volta che il campo viene rimosso. In pratica, è la condizione ideale per un agente di contrasto: le nanoparticelle si allineano rapidamente al campo magnetico generato dalla macchina MRI, aumentando il contrasto dell’immagine, e poi tornano neutre, evitando qualsiasi effetto indesiderato. Test di rilassometria condotti a diverse frequenze hanno confermato tempi di risposta molto rapidi, dell’ordine di miliardesimi di secondo, perfettamente compatibili con i requisiti clinici.
Un aspetto decisivo dello studio riguarda la sicurezza biologica, condizione essenziale per qualsiasi applicazione medica. Per verificarla, il gruppo ha condotto esperimenti su linee cellulari di macrofagi, cellule del sistema immunitario che hanno il compito di individuare e distruggere corpi estranei. Queste cellule rappresentano un modello affidabile per valutare la compatibilità di nuovi materiali. I risultati hanno mostrato che, anche a concentrazioni elevate di nanoparticelle, la vitalità cellulare rimane superiore al 70 per cento dopo 24 ore di esposizione, un valore pienamente conforme agli standard internazionali di sicurezza (ISO 10993-5). Le nanoparticelle si sono dimostrate stabili anche in soluzioni contenenti proteine e albumina, simulando il sangue umano, senza segni di degradazione o aggregazione. Ciò significa che il materiale potrebbe circolare nell’organismo senza accumularsi né interferire con i processi fisiologici.
L’aspetto forse più interessante di questa ricerca è che l’innovazione non consiste nella scoperta di un nuovo materiale, ma nel modo in cui viene prodotto. L’uso combinato di microonde e ultrasuoni consente infatti di ridurre i tempi di reazione da diverse ore a pochi minuti, con un notevole risparmio energetico. Inoltre, il processo non richiede solventi organici tossici né alte temperature, rispettando i principi della chimica sostenibile, o “green chemistry”. Questo rende il metodo facilmente replicabile e adattabile su scala industriale, aprendo la possibilità di produrre materiali di alta qualità a costi ridotti. È un esempio di come la ricerca di base, condotta in laboratorio, possa tradursi in applicazioni concrete in grado di migliorare la sicurezza, la sostenibilità e l’efficienza della diagnostica medica.
Oltre all’impiego come agenti di contrasto per la risonanza magnetica, le nanoparticelle sviluppate dal team dell’Università di Torino aprono prospettive più ampie. Grazie alla presenza della β-ciclodestrina, possono essere utilizzate come piattaforme per la somministrazione controllata di farmaci, capaci di rilasciare principi attivi solo dove e quando serve. Questa doppia funzione – diagnostica e terapeutica – le rende un esempio di “teranostici”, un termine che indica materiali capaci di unire diagnosi e cura in un unico sistema. In futuro, questi sistemi potranno essere impiegati non solo per migliorare la precisione delle immagini mediche, ma anche per intervenire direttamente sui tessuti malati, riducendo effetti collaterali e dosi farmacologiche. Le loro caratteristiche di stabilità e biocompatibilità aprono inoltre prospettive nel campo dell’ingegneria tissutale e delle terapie fototermiche, in cui le nanoparticelle vengono riscaldate con la luce per distruggere selettivamente cellule tumorali.
Nel complesso, il lavoro di Federica Calsolaro, Francesca Garello, Eleonora Cavallari, Giuliana Magnacca, Mikhail V. Trukhan, Maria Carmen Valsania, Giancarlo Cravotto, Enzo Terreno e Katia Martina rappresenta un esempio di eccellenza scientifica italiana, capace di coniugare rigore accademico, creatività tecnologica e attenzione alla sostenibilità. Il progetto, realizzato nell’ambito del nodo italiano di EuroBioImaging e sostenuto dal Ministero dell’Università e della Ricerca tramite i fondi FOE, conferma la centralità della collaborazione tra discipline diverse – chimica, fisica e biologia – nella costruzione della medicina del futuro. Le nanoparticelle non sono solo un nuovo materiale, ma un segno concreto di come la scienza possa unire diagnosi, terapia e sostenibilità in un’unica direzione: rendere la medicina più precisa, meno invasiva e più vicina alla persona.
L’articolo è parte dei servizi per la Terza Missione che Stroncature produce per conto del Dipartimento di Chimica dell’Università di Torino